اسید آمینه
اسید آمینه در شیمی به هر ملکولی که شامل گروههای کاربردی آمینه و کربوکسیلیک اسید است گفته میشود. اسید آمینه واحد تشکیل دهنده پروتئین است. اسیدهای آمینه در هنگام ساخته شدن پروتئینها از RNA پیامبر یا mRNA به یکدیگر میپیوندند.
در بیوشیمی به اسیدهای آلفا آمینو یعنی آن اسید آمینههایی که در آنها کارکردهای آمینو و کاربوکسیلات هر دو به کربنی یگانه چسبیدهاند اسید آمینه میگویند.

ساختار اسیدهای آمینه
هر اسید آمینه، از یک کربن نامتقارن به نام کربن α تشکیل یافتهاست که با چهار گروه مختلف کربوکسیل (COOH) اتم هیدروژن، گروه آمینه بازی (NH۲-) و یک زنجیره غیر جانبی (R-) پیوند برقرار میکند. ریشه R ممکن است یک زنجیره کربنی و یا یک حلقه کربنی باشد. عوامل دیگری مانند الکل، آمین، کربوکسیل و نیز گوگرد میتوانند در ساختمان ریشه R شرکت کنند. زنجیره جانبی خود چندین اتم کربن دارد و آنها را به ترتیبی که از کربن آلفا، فاصله میگیرند، با حروف بتا (β)، گاما (γ) و دلتا (δ) نشان میدهند. اگر در حالی که عامل COOH روی کربن آلفا قرار داد عامل NH۲ روی کربنهایی غیر آلفا قرار گیرد. نوع اسید آمینه به β، γ یا δ تغییر خواهد کرد. اسیدهای آمینه آزاد به مقدار بسیار ناچیز در سلولها وجود دارند. بیشتر اسیدهای آمینه آلفا در سنتز پروتئین شرکت میکنند، در صورتی که اسیدهای آمینه بتا، گاما و دلتا واسطههای شیمیایی هستند. بیشتر اسیدهای آمینه در pH هفت به صورت دو قطبی در میآیند یعنی گروه NH۲ پروتون میگیرد و گروه COOH هیدروژن خود را از دست میدهد و به صورت –COO- در میآید. زنجیره جانبی (گروه) R برای پروتئینها میتواند یکی از ۲۰ حالت مختلف ممکن باشد و بدین ترتیب یک الفبای بیست حرفی برای ساخت پروتئینها بوجود میآید. این بیست اسید آمینه میتوانند با هر ترکیب و به هر تعداد در ساختار یک پروتئین دخالت کنند.
ایزومری در اسیدهای آمینه
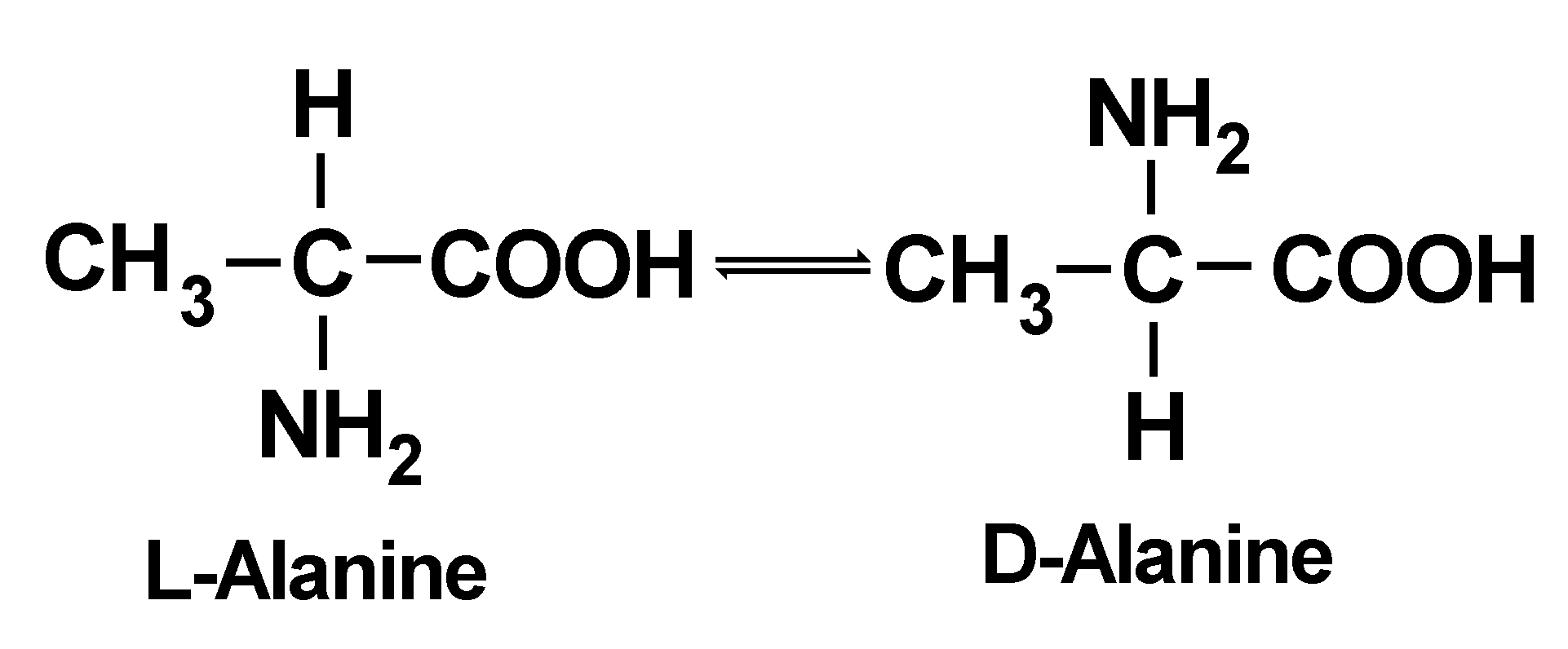
دو ایزومر نوری آلانین
مطابق قرار داد اگر ساختمان فضایی یک اسید آمینه را در نظر بگیریم، چنانچه عامل NH۲ که به کربن آلفا متصل است در طرف چپ باشد، میگوییم که این اسید آمینه از نوع L است و هرگاه عامل NH۲ در طرف راست کربن آلفا قرار گیرد، گوییم که این اسید آمینه از نوع ∆ است. برخلاف قندهای طبیعی که از نوع ∆ هستند، اسیدهای آمینه طبیعی همگی از نوع L هستند. این ایزومرهای نوری را ایزومرها را انانتیوم میگویند.
ساختار و نماد تعدادی از اسید آمینه
بیست نوع اسید آمینه در تشکیل پروتئینها شرکت دارند. بر اساس گروه R متصل به آنها و در نتیجه خواص شیمیایی آنها، این بیست اسید به سه گروه تقسیم میشوند. این سه گروه عبارتند از:
هیدروفوبیک
قطبی
بار دار (مثبت و منفی(
در هریک از این دستهها میتوان زیر دستههایی با جزئیات بیشتر تعریف نمود. مانند آروماتیک یا الیفاتیک، کوچک یا بزرگ، و غیره.

خلاصه :
اسید های آمینه زیر واحد های پروتئین ها هستند و از 20 نوع تشکیل شده اند که تعدادی از آن ها ضروری نام دارند. بدین معنا که بدن توانایی ساختشان را ندارد و باید آن ها را جز رژیم غذایی مصرف کرد. تعدادی از آمینو اسید ها فعالیت نوری دارند که این فعالیت به دلیل پدیده ایزومری است.
لطفا اندیشه و نظر خود را در قسمت نظرات اعلام کرده و بنویسید.
- ۹۳/۰۳/۲۲

